La
criptosporidiosis es una
enfermedad oportunista causada por el
parásito Cryptosporidium, presente en algunas comidas o en agua contaminada. El primer caso reportado se presentó en 1972, y a partir de entonces es uno de los patógenos a nivel de vía entérica más comunes en el mundo (además de la Giardiosis). En 1993, en la ciudad de
Milwaukee,
Wisconsin,
Estados Unidos; se presentó un brote de infección por
Cryptosporidium que dejó un saldo de alrededor de 403.000 personas.
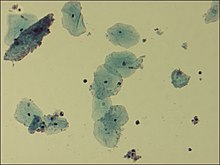
Agente patógeno
El
Cryptosporidium es un patógeno de carácter intracelular perteneciente al reino
protista, subreino
protozoo, filo
apicomplexa y grupo alveolara. Alrededor de 20 especies de este agente son reconocidos actualmente. La especie de
Cryptosporidium más común en humanos es
C. parvum (que cuenta con dos genotipos, el tipo 1 es el humano y el tipo 2 es el bovino), aunque en pacientes inmunosuprimidos se han hallado
C. hominis,
C. muris,
C. felis y
C. meleagridis. El parásito es de tipo
monoxenes (es decir, capaz de desarrollar todas sus etapas del ciclo de vida en un solo hospedero) y posee un ciclo de vida bastante complejo.
[editar] Epidemiología
La infección es autolimitada en personas inmunocompetentes pero potencialmente letal en pacientes inmunosuprimidos. Del 1 al 3 por ciento de los habitantes de países en vía de desarrollo excretan ooquistes de
Cryptosporidiumen heces fecales. En promedio, el 2,2 por ciento de los habitantes de países tercermundistas que tienen enfermedades diarreicas poseen Criptosporidiosis. El 7% de los niños habitantes de países industrializados (como Estados Unidos y Canadá) que sufren de diarrea padecen Criptosporidiosis, mientras que el 12 por ciento de los infantes habitantes de países en vía de desarrollo que tienen ataques diarreicos poseen infección por Cryptosporidium.
Con respecto a los pacientes con Síndrome de Inmunodeficiencia Adquirida (SIDA) y diarrea al mismo tiempo; el 12% pacientes con dichas condiciones (siendo habitantes de países industrializados) poseen Criptosporidiosis, mientras que el 24% de los pacientes con las condiciones anteriormente mencionadas (siendo habitantes de países en vía de desarrollo) poseen infección por dicho agente pátógeno.
Los
factores de riesgo para Criptosporidiosis son: Habitantes del hogar de uno o más enfermos de infección por Cryptosporidium, parejas sexuales del paciente enfermo, trabajadores de la salud, personal de guarderías, usuarios de piscinas públicas y viajeros de zonas no endémicas que llegan a zonas endémicas
La infección se puede trasmitir por
vía sexual anal u oral (contacto orofecal), por nadar en aguas contaminadas con heces humanas, por consumir ostras en mal estado, por consumir agua contaminada y/o por haber tenido contacto con fómites (fuentes de contagio inanimados) como el agua contaminada y el vómito de un paciente con dicha infección.
[editar] Inmunología
En la defensa de la infección por
Cryptosporidium es importante tanto la inmunidad celular como la humoral. La invasión de células epiteliales
in vitro con
Cryptosporidium otorga como resultado la producción de
citoquinas proinflamatorias, importante en la defensa temprana en dicha infección. Las células epiteliales infectadas por
cryptosporidiumproducen péptidos antimicrobianos (como las beta-defensinas) y/o prostaglandina E2 con el fin de evitar una invasión parasitaria. Diversos estudios han demostrado la importancia del IFN-γ en la defensa del hospedero, puesto que un déficit en dicha citoquina en ratones knock-out y en humanos provoca una mayor susceptibilidad a sufrir de Criptosporidiosis.
La resistencia adquirida a dicho parásito depende de los linfocitos T con receptores para células T α/β, y adicionalmente se ha comprobado un papel protector en el linfocito T CD4+. Al parecer, los linfocitos T CD8 y los linfocitos γ/κ son poco importantes en la defensa del huésped. En infecciones agudas y en pacientes convalescientes se han encontrado niveles elevados de IgA, IgG, IgM e IgE en suero plasmático. Los mecanismos por los cuales las células del epitelio gastrointestinal provocan la respuesta inmunológica no son muy bien comprendidos.
[editar] Signos y síntomas
Aunque la infección puede ser asintomática, en la mayoría de pacientes con Criptosporidiosis presentan diarrea acuosa con presencia de moco. Es raro encontrar en heces fecales la presencia de sangre o leucocitos. La duración de los signos y síntomas de dicha enfermedad dependen en gran parte del estado inmunológico del paciente. En un paciente inmunocompetente, la enfermedad tiene una duración media de 7 a 10 días, mientras que en un paciente inmunosuprimido la enfermedad (dependiendo del conteo de linfocitos T CD4+) puede presentarse de manera asintomática o sufrir los síntomas por el resto de su vida.
Los
signos y síntomas que presenta normalmente las personas inmunocompetentes son:
diarrea acuosa con presencia de moco, fiebre, náuseas, vómito, dolor abdominal (calambre) y pérdida de peso; mientras que los pacientes inmunosuprimidos son fiebre, dolor en el cuadrante superior derecho del abdomen, vómito, pérdida de hasta el 10% del peso corporal,
ictericia y malabsorción severa. En el brote de
Cryptosporidium de 1993, el número máximo de deposicíones por día fueron de 12 y la duración media de la enfermedad fué de 12 días.
Las
formas de presentación clínicade la Criptosporidiosis en personas inmunocompetentes son: Portador asintomático, diarrea aguda y diarrea persistente (por aproximadamente un par de semanas); mientras que en pacientes inmunosuprimidos las diferentes formas de presentación clínica son: Enfermedad asintomática, enfermedad transitoria, enfermedad crónica y enfermedad fulminante. La siguiente tabla muestra el conteo de linfocitos T CD4+ en personas inmunosuprimidas y la presentación clínica que comúnmente presentan:
| Conteo de linfocitos T CD4+ | Presentación clínica |
|---|
| > 200/mm3 | Enfermedad asintomática |
| < 100/mm3 | Enfermedad crónica |
| < 50/mm3 | Enfermedad fulminante |
La Criptosporidiosis extraintestinal se ha reportado en pacientes inmunosuprimidos, y los lugares más frecuentes de aparición de Cryptosporidiumson: Conducto biliar, pulmones, estómago y páncreas. Dichos sitios son probablemente extensiones de la infección primaria. La verdadera frecuencia de Criptosporidiosis extraintestinal no se ha podido determinar, puesto que las pruebas diagnósticas para detectar Cryptosporidiuma nivel extraintestinal requieren de métodos invasivos. Al presentarse síntomas de enfermedad biliar durante el transcurso de la enfermedad hay un número menor de linfocitos T CD4+ en el conteo. Aunque la Criptosporidiosis biliar contribuye a la naturaleza crónica de la infección y por supuesto aumenta la morbilidad en pacientes con VIH, al parecer no se presenta un aumento de la mortalidad de los mismos.
[editar] Diagnóstico
Se debe tener en cuenta el diagnóstico de Criptosporidiosis en pacientes que presentan diarrea aguda o persistente, especialmente en personas inmunosuprimidas (sea por SIDA o por otra causa). El diagnóstico definitivo requiere de la observación microscópica del parásito a nivel de tejidos o fluídos corporales, aunque los métodos clínicos, endoscópicos, inmunológicos y moleculares todos toman un papel en el diagnóstico. Actualmente se realiza un exámente de tinción ácidoresistente modificada para determinar la presencia de
Cryptosporidium en la muestra. La
sensibilidad y
especificidad de dicha prueba ha mejorado gracias a los métodos inmunológicos, como el ensayo de inmunofluorescencia directa y el ensayo inmunoenzimático (ELISA). La pueba de la reacción en cadena de la polimerasa (PCR) está disponible para detectar
Cryptosporidiuma nivel investigativo. Los trabajadores de la salud deben de tener en cuenta que los examenes de rutina para hallar parásitos (ova plus parasite) no detectan Criptosporidiosis, por lo que es recomendable ordenarse una prueba específica para Cryptosporidium. Las pruebas serológicas de Cryptosporidium no son de gran utilidad, puesto que muchas personas sanas poseen anticuerpos para dicho parásito.
Al haber sospecha de enfermedad biliar, la mejor prueba de diagnóstico inicial es la
ecografía por
ultrasonido, mediante el cual se puede detectar el engrosamiento del conducto biliar y/o la dilatación de la vesícula biliar. Si la sospecha de enfermedad biliar continúa a pesar de que la ecografía por ultrasonido arroja resultados normales, lo ideal es ordenar al paciente una
colangiopancreatografía retrógrada endoscópica (usada en pacientes con el VIH-1) puesto que posee mayor sensibilidad. El patrón angiográfico más común (en el 50-60% de los pacientes) es la estenosis papilar asociada a colangitis esclerosante intrahepática. Otros patrones angiográficos son estenosis papilar sola, colangitis esclerosante sin estenosis papilar y estenosis largas de los conductos biliares extrahepáticos. La ecografía endoscópica es útil en la detección de estenosis papilar y superior a la ecografía transabdominal, y se usa para descartar otras condiciones como cálculos, compresión o cáncer. La biopsia hepática percutánea, aunque usada comúnmente, no es importante para el diagnóstico.
[editar] Tratamiento
No existe en la actualidad tratamiento eficaz contra la Criptosporidiosis. No hay ningún agente antimicrobiano ni quimioterapéutico que sea lo suficientemente eficaz para erradicar al organismo de forma fiable. Sin embargo, hay agentes que parecen suprimir la infección. En pacientes con VIH, el uso de la terapia antirretroviral de alta actividad puede resolver los síntomas de la Criptosporidosis. Algunos nucleósidos antivirales tienen un efecto directo en el crecimiento de Cryptosporidium in vitro. Puesto que el curso clínico de la enfermedad depende en gran medida el estado inmunológico del paciente, las opciones de tratamiento pueden variar. Por lo general los pacientes inmunosuprimidos de carácter asintomático no necesitan un tratamiento específico. La administración al paciente de electrólitos y fluidos por vía parenteral u oral permite recuperar el estado hídrico tras los sucesos continuos de diarrea. En niños, la
espiramicina puede acortar la duración de la excreción de ooquistes y diarrea, aunque los datos presentados presentan conflicto. En pacientes con SIDA se usa la terapia antirretroviral de alta actividad, y si con lo anterior los síntomas no mejoran, el tratamiento estándar sería una combinación de dicha terapia con la administración conjunta de un antidiarreo y un antimicrobiano. La
paromomicina y la
azitromicina y la
nitazoxanidason comúnmente usados, aunque dichos medicamentos son moderadamente efectivos. En pacientes con inmunodeficiencias debe descartarse la presencia de otros agentes patógenos. El mejor tratamiento para la Criptosporidiosis biliar en pacientes con SIDA es la terapia antirretroviral de alta actividad. Aunque dicho tratamiento resuelve la infección, no es posible erradicar al organismo del cuerpo. En caso de no resolver la infección, se usan vías endoscópicas (como la esfinterectomía endoscópica) que aunque no se prolonga la supervivencia, otorga una mejor calidad de vida en pacientes con estenosis papilar y colangitis esclerosante o simplemente estenosis papilar. Los pacientes con sólamente colangitis esclerosante (extrahepática o intrahepática) tienen pocas opciones a nivel terapéutico específico. Los fármacos antiparasitarios no suelen ser efectivos contra la Criptosporidiosis biliar en pacientes con SIDA y colangiopatía.
[editar] Prevención
Como la infección por
Cryptosporydium se da exclusivamente por la ingesta de ooquistes, las medidas de control apuntan a reducir o prevenir la transmisión de ooquistes. Los ooquistes son muy resistentes a una gama de presiones ambientales y a la mayoría de desinfectantes y antisépticos. La filtración de agua no remueve todos los quistes de
Cryptosporidium, por lo que lo ideal es que las plantas de tratamiento de agua realicen una revisión microscópica de rutina. Las personas inmunosuprimidas deben evitar tener contacto con agua no potable (lagos y arroyos) y animales jóvenes. En los hospitales y centros de salud, los pacientes infectados deben de evitar tener contacto con las fuentes de infección y además aislarse de los demás pacientes. Para prevenir una posible infección por agua de dudosa potabilidad, lo recomendable es hervir el agua antes de su consumo.

 Aviso médico
Aviso médico